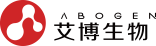The human body produces and utilizes numerous proteins to carry out essential biological functions, including growth, development, cellular repair and maintenance. With over 100,000 types of proteins performing diverse roles, precise regulation of protein production is fundamental to health.
Messenger ribonucleic acid (mRNA), transcribed from DNA, delivers instructions to ribosomes, playing an essential role in regulating protein synthesis. With cutting-edge technologies, scientists can design mRNA-based therapeutics that is revolutionizing treatments for diseases beyond the reach of traditional therapies.
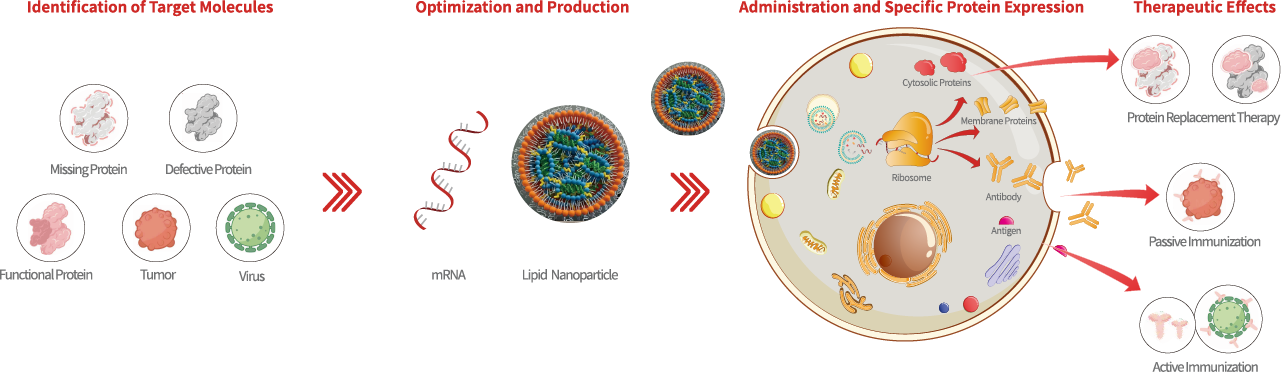
mRNA technology has been in development since the 1960s, but it did not gain significant attention until recent years. For over half a century, three major challenges, including the safety and druggability of mRNA, delivery efficiency and scalable manufacturing, have been hindering mRNA-based drug discovery. Nowadays, its success in combating the pandemic has revitalized interest in developing mRNA-based therapeutics. As we look back, all the milestones and breakthroughs of mRNA science and technology are jointly laying a solid foundation for this medical revolution.
With years of pioneering mRNA research, Abogen has always been pursuing a vision beyond therapeutic development — making mRNA drug discovery more efficient, effective and safer. On the journey to this great expectation, our proprietary innovative mRNA technology platform is our solid foundation.
Abogen is currently one of the very few mRNA biotech companies worldwide with integrated cutting-edge technologies in-house to support full-cycle development of mRNA medicines, from target selection and mRNA optimization to GMP production and clinical delivery.
The platform serves as an engine powering our relentless exploration in mRNA research and development. Building on its proven efficacy in large-scale Phase III clinical trials, we continue to enhance its capabilities, fostering the establishment of a diversified pipeline spanning immuno-oncology, protein replacement therapies, and infectious disease prevention.
-
 RNA design, synthesis and modificationSynthetic modified mRNA molecules are key to mRNA-based therapeutics. They carry critical information to produce antibodies or antigens to fight or prevent diseases.Leveraging state-of-the-art computational system powered by AI, we design mRNA sequences to achieve high protein translation efficiency, enhancing the effectiveness of mRNA therapeutics. Along with the proprietary modification technology to mitigate mRNA-induced innate immunity, we have also established fully automated mRNA synthesis and quality control technologies for mRNA, self-amplifying RNA (saRNA) and circular RNA (circRNA), with exceptional quality, consistency, efficacy and safety.
RNA design, synthesis and modificationSynthetic modified mRNA molecules are key to mRNA-based therapeutics. They carry critical information to produce antibodies or antigens to fight or prevent diseases.Leveraging state-of-the-art computational system powered by AI, we design mRNA sequences to achieve high protein translation efficiency, enhancing the effectiveness of mRNA therapeutics. Along with the proprietary modification technology to mitigate mRNA-induced innate immunity, we have also established fully automated mRNA synthesis and quality control technologies for mRNA, self-amplifying RNA (saRNA) and circular RNA (circRNA), with exceptional quality, consistency, efficacy and safety. -
Lipid nanoparticle (LNP) delivery systemEfficient delivery requires mRNA to be protected from degradation. With extensive expertise in lipid nanoparticle (LNP) science, we have established a proprietary, industry-leading LNP delivery platform.Our own ionizable lipid has been validated in large-scale phase III clinical trials, with patent granted in China, the U.S., Australia and major European countries. We have further developed an AI-driven proprietary ionizable lipid library and a molecular database encompassing 30 million lipid structures, enabling the generation of novel lipids with favorable safety and efficacy profiles.

-
Clinical & commercial manufacturing platformOur proprietary Dynamic Precision Mixing (DPM) technology produces highly safe and uniform LNPs with high mRNA encapsulation efficiency during scale-up and ensures stable formulations at 2–8 °C. The product quality, safety and stability have been proven in a global Phase III trial enrolling over 30,000 participants. With manufacturing certificates and commercial-scale production facilities, we are among the few mRNA companies worldwide with comprehensive, scalable in-house manufacturing capabilities.Our advanced lyophilization capabilities also enhance the stability and cost-effectiveness of storage, making mRNA therapeutics more accessible worldwide.
-
AI platformAdvanced AI technologies are seamlessly integrated into every stage of mRNA drug development to enhance precision, efficiency and efficacy, including protein engineering, mRNA optimization, immunogenic neoantigens prediction, ionizable lipid formulation and screening.Through the strategic deployment of AI, we are not only enhancing both the speed and effectiveness of our drug discovery process, but also evolving into a digital, AI-driven biotech company with a vision for the future.